RESÚMENES
Progresión del tratamiento tras la insulina basal: agonistas del GLP-1 frente a la insulina prandial y frente a la insulina premezclada
Presentado por:Helena W. Rodbard, MD, FACP, MACE
Medical Director, Endocrine and Metabolic Consultants
Rockville, MD; USA
La inercia clínica es preocupante en los pacientes con diabetes tipo II dada la clara relación que existe entre el control deficiente de la glucemia y las complicaciones de esta enfermedad. Un elemento crítico de la inercia clínica es el frecuente retraso entre el inicio de la insulina basal y la intensificación del tratamiento1. De los pacientes que recibieron dicha insulina, solo al 30,9 % de aquellos cuya HbA1c aumentó a ≥7,5 % se les intensificó el tratamiento y solo el 20,9 % alcanzó niveles de HbA1c <7,5% en 6 meses1.
Las opciones de intensificación, según el algoritmo de la ADA, son los agonistas del receptor del GLP-1, la insulina y la insulina premezclada2. Revisaremos con detalle cada una de ellas.
La farmacocinética de los agonistas del receptor del GLP-1 puede ser de acción corta o prolongada. Los fármacos de acción corta son exenatida dos dosis al día, lixenatida una vez al día y liraglutida una vez al día, con vida-media de 2.4, 3 y 13 horas, respectivamente3. Los de acción prolongada son dulaglutida una vez por semana, exenatida una por semana y semaglutida una por semana, con vida media de ~4 días, 7-14 días y ~7 días, en ese orden3.
En un estudio que añadió lixisenatida a insulina basal en pacientes con control deficiente de diabetes de tipo II, se observaron beneficios adicionales4. El nivel medio de la HbA1c bajo a 7.8 % en comparación con 8.1 % del grupo control, al igual que la variación media del peso corporal (–1.3 kg frente a –0.01 kg). También se observó un descenso en las unidades medias de insulina (50 frente a 57)4. Las variaciones de la glucemia plasmática en ayunas no fueron evidentes ni se esperaban con un agonista del receptor del GLP-1 de acción corta4. También se observó una mejora en la curva glucémica de 7 puntos (antes del desayuno, 2 horas después del mismo, antes de la comida, 2 horas después de la misma, antes de cenar, 2 horas después de la cena y antes de acostarse) en el grupo de lixisenatida en comparación con placebo4.
El estudio AWARD-9 analizó el uso de dulaglutida 1.4 mg una vez a la semana + insulina glargina (IGlar) una vez al día frente al de placebo + IGlar una vez al día en pacientes con diabetes tipo II5. Para participar, los pacientes debían seguir un tratamiento con insulina basal ± metformina y tener niveles de la HbA1c ≥7,0 % y ≤10,5 %5. El grupo dedulaglutida experimentó una reducción estadísticamente significativa de la HbA1c de –1.44 % frente al –0.67% del placebo, p <0,001), además de una reducción del peso corporal de –1.91 kg frente a +0.50 kg con el placebo (p <0,001)5.
El estudio SUSTAIN 5 publicado recientemente examinó semaglutida añadida a insulina basal en pacientes con diabetes tipo 26. Incluyó a poco menos de 400 pacientes con niveles de la HbA1c entre el 7.0 % y 10 % que seguían un tratamiento estable con insulina basal sola o acompañada de metformina6. Se estudiaron dos dosis de semaglutida: 0.5 y 1 mg6. La variación media de la HbA1c respecto al inicio alcanzó la significia estadística con ambas dosis de semaglutida (–1.3 y –1.7 %, respectivamente, p <0,001) en comparación con placebo (–0.2)6. También se observó una disminución de la variación del peso corporal medio respecto al inicio con ambas dosis de semaglutida en comparación con el placebo (–7.7 lb (–3.5 kg), –13.2 lb (–6 kg), –2.6 lb (1.2 kg) con 0,5 mg, 1,0 mg de semaglutida y con placebo, en ese orden)6.
En el ensayo LixiLan-L, una combinación que permitía ajustar la dosis en proporciones fijas de IGlar y lixisenatida en pacientes con diabetes tipo II demostró mejoras en la reducción de la HbA1c, en el número de pacientes que alcanzaron la meta de HbA1c, y en la variación de peso en comparación con los que solo recibieron IGlar7. Los tratados con la combinación de lixisenatida también experimentaron un menor porcentaje de episodios de hipoglucemia y sufrieron menos episodios de ese tipo por año que los receptores de IGlar sola7.
El último estudio analizado era un ensayo que valoró la eficacia y la seguridad de la liraglutida una vez al día + insulina glargina (IdegLira) frente al régimen de insulina basal-bolo en pacientes con diabetes tipo II que no estaban controlados con metformina einsulina basal8. Más de 500 pacientes se aleatorizaron para recibir IDegLira + metformina o bien IGlar + insulina aspart (IAsp) + metformina. Para participar, se debía tener una HbA1c entre el 7.00 y el 10.0 %8. Se observó significación estadística en la proporción de pacientes tratados con IDegLira que alcanzaron una HbA1c <7 % sin ganancia de peso, en la proporción de los que lograron una HbA1c <7 % sin sufrir hipoglucemia, y en la proporción de los que alcanzaron una HbA1c <7 % sin hipoglucemia y sin ganancia de peso en comparación con el grupo de la IGlar8. No se alcanzó la significación estadística en el número de pacientes que únicamente alcanzaron una HbA1c <7 %8.
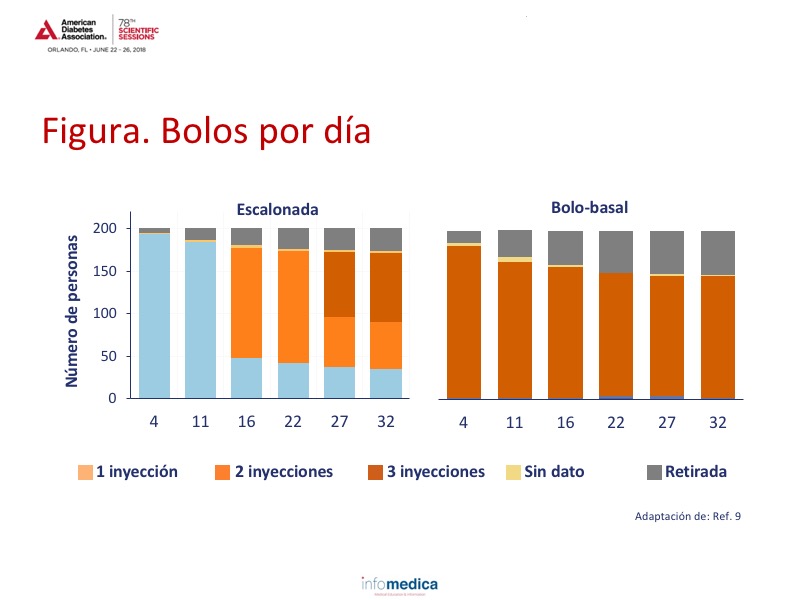
El estudio FullSTEP se diseñó para averiguar si, cuando se precisaba intensificar el tratamiento con insulina en bolo, era tan efectiva la adición gradual de la IAsp (una dosis prandial antes de la comida principal) como comenzar con 3 dosis en bolo9. Para participar, los pacientes debían tener diabetes de tipo II desde hacía al menos 12 meses, aplicarse insulina basal desde al menos 6 meses antes y presentar una HbA1c entre 7.0 y 9.0%9. Los objetivos glucémicos consistieron en una glucemia plasmática en ayunas de 71-130 mg/dl y una HbA1c <7 %9. Los participantes se estratificaron según de los intervalos de HbA1c 7.0 %-8.0 % y 81 %-9.0 %9. Los integrantes del grupo de bolo-basal recibieron IAsp preprandial; los del grupo de dosis escalonadas recibieron 1 dosis prandial con la comida principal acompañada de dosis adicionales de IAsp antes de la siguiente comida principal a las 11 y a las 22 semanas si la HbA1c se mantenía en 7 % o por encima de ese valor. Durante el período de 33 semanas, la HbA1c media disminuyó del 7.9 % al 6.9 % en el grupo de escalonamiento y del 7.9 % al 6.8 % en el grupo de bolo-basal (p = 0,88)9. Cabe destacar que en este último grupo los pacientes que abandonaron el estudio fueron el doble que en el grupo de escalonamiento de dosis, lo que demuestra mejor tolerabilidad y la mayor satisfacción del paciente9. Consulte la figura.
Los pacientes del grupo de dosis escalonadas también tuvieron tasas más bajas de hipoglucemia que los sometidos al régimen bolo-basal, tanto en el total de episodios como en los sintomáticos comprobados, los asintomáticos, los no clasificables según ADA y los nocturnos, muchos en una relación relativa de 2:19.
En un ensayo clínico se estudió la eficacia y la seguridad de dos estrategias de intensificación del régimen de insulina destinadas a pacientes con diabetes tipo 2 que ya habían recibido insulina basal: IDeg e IAsp administradas como una coformulación dos veces al día o en régimen basal-bolo (inyecciones independientes)10. Ni la reducción de la HbA1c ni la incidencia de la hipoglucemia mostraron la significación estadística al comparar los resultados de IDeg-Asp y de IDeg + IAsp por separado10.
Mensajes clave
- A menudo se retrasa mucho la intensificación del tratamiento con insulina incluso cuando el paciente está por encima de los objetivos de control glucémicos.
- Los agonistas del receptor del GLP-1 pueden ser de acción corta o de acción prolongada y han demostrado ser eficaces al reducir HbA1c a los niveles objetivo, disminuyendo peso y disminuyendo riesgo de hipoglucemia cuando se usan en combinación con insulina.
- Añadir progresivamente bolos de insulina de acción rápida reduce la HbA1c y el riesgo de hipoglucemia respecto al régimen bolo-basal.
- La administración de la insulina premezclada reduce la HbA1c y la tasa de hipoglucemia en la misma proporción que el tratamiento bolo-basal.
REFERENCIAS
Declaraciones de los ponentes: La ponente declara haber sido asesora de Bayer, BI/Lilly, Janssen, Lexicon, Merck, Novo Nordisk, Sanofi y Regeneron. También es conferenciante de Astra Zeneca, BI/Lilly, Merck, Novo Nordisk y Sanofi y presta apoyo a la investigación para Astra Zeneca, BI/Lilly, Janssen, Lexicon, Merck, Mylan, Novo Nordisk, Sanofi y Regeneron.
Escrito por: Debbie Anderson, PhD
Revisado por: Marco Gallo, MD